葛磊医生的科普号
- 案例 腹腔镜
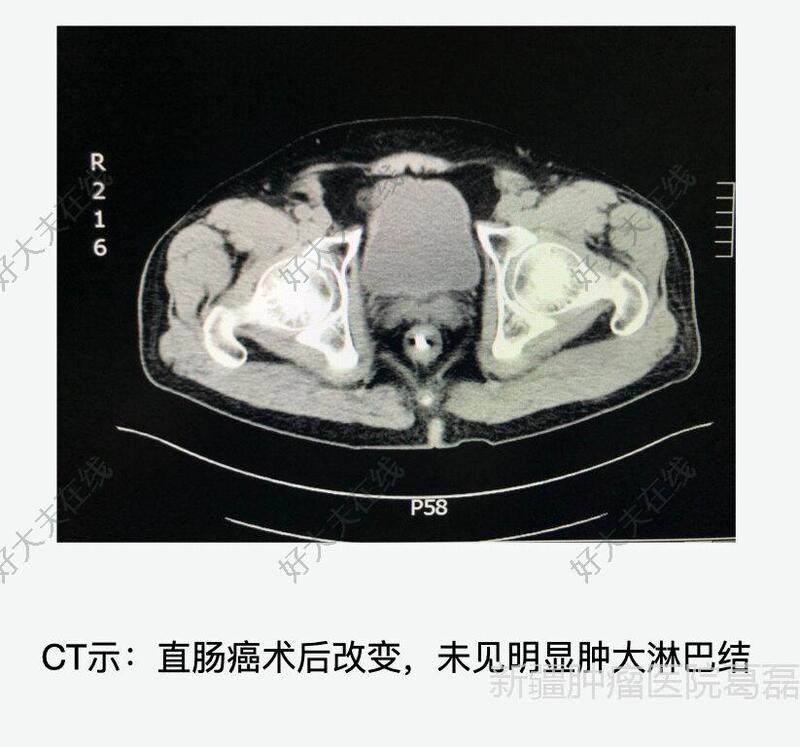
治疗前患者男性,59岁,外院肠镜检查提示:距肛门5cm可见大小约1.21.0cm肿瘤,行肠镜下切除术后,病理提示:直肠中分化腺癌,浸润黏膜下层,切缘距离黏膜下层小于0.5mm。NRAS突变型。治疗中手术中进行微创切除,注意患者神经功能保护,尤其是男性患者排尿功能和性功能的保护。治疗后治疗后1天手术情况:手术时间:245分钟术中出血量:50ml患者术后腹部无切口,两根引流管引流。术后16小时下地活动。术后经口饮水。第二天流质饮食
 葛磊 主任医师 广东医科大学附属医院 胃肠外科106人已读
葛磊 主任医师 广东医科大学附属医院 胃肠外科106人已读 - 诊前须知 胃癌术后常见问题的管理--患者的五种常见问题
医生,喉咙很不舒服,什么时候可以拔胃管?我可以坐起来吗?什么时候可以下床活动?什么时候可以吃东西?这个引流管什么时候可以拔?面对上述问题,我们将在日常管理中总结胃癌术后的常规处理,主要针对麻醉残余作用、手术创伤以及康复过程中可能出现的异常情况,预防和及时发现手术并发症以便及时处理,协助患者顺利康复。
葛磊 主任医师 广东医科大学附属医院 胃肠外科510人已读 - 诊后必读 胃大部切除术后患者饮食注意原则葛磊 主任医师 广东医科大学附属医院 胃肠外科1人已购买
- 诊后必读 胃癌术后护理注意事项葛磊 主任医师 广东医科大学附属医院 胃肠外科暂无购买
- 医学科普 “五心”胃癌防治葛磊 主任医师 广东医科大学附属医院 胃肠外科761人已读
- 案例 完全腹腔镜胃肿瘤切除
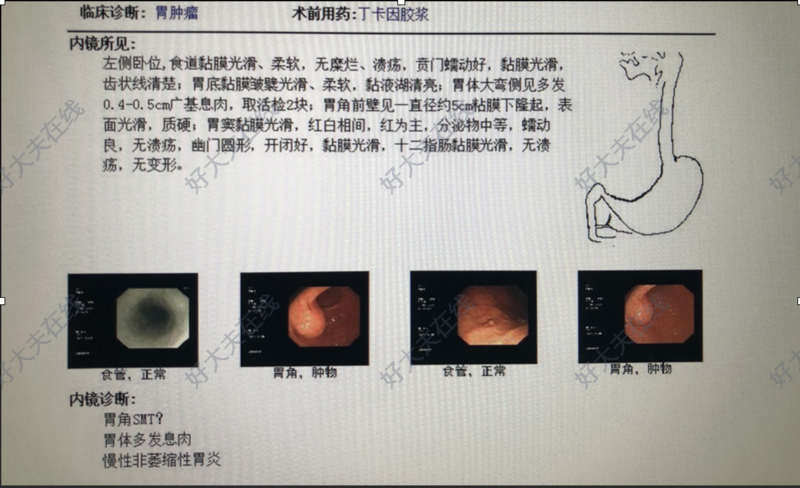
治疗前 患者女性,粘膜下肿物生长,部分肿物生长突出浆膜外,考虑腹腔镜微创治疗。 治疗后 治疗后30天 三、鉴别诊断 1. 胃的胃肠间质瘤(gastrointestinal stromal tumor,GIST):起源于一种具有多向分化潜能的间质干细胞,主要成分是梭形细胞(70-80%),类上皮细胞(20-30%)。GIST可发生于消化道的任何部位,多见于胃(60~70%)和小肠(20~30%),结直肠(10~20%),食管(0~6%),肠系膜、大网膜及腹膜后罕见。常发生于50岁以上中老年人。病变多为单发,密度不均,内部出血、坏死、囊性变多见增强时肿块呈不均匀强化。免疫组化为CD117、CD34阳性而S-100及GFAP多为阴性。 2. 胃神经鞘瘤(gastric schwannoma,GS):好发于胃体部,其次为胃底,胃窦部少见可向腔内、腔外或同时骑跨腔内外生长。多为单发壁内起源的圆形、椭圆形或分叶肿块,边界清楚。肿瘤直径多小于 5 cm,内部结构比较均匀,很少出现坏死及钙化,低密度区通常代表肿瘤内部的坏死、囊变、陈旧出血或神经鞘瘤富含Antoni B型细胞区。可有小溃疡形成龛影,其特征是浅表、直径小、发生于胃腔内面的特点;有合并脓肿并继发胃穿孔的个案报道。CT平扫肿瘤呈等或稍低密度影,密度均匀,分界清楚,较少发生钙化或囊变[4]。增强后肿瘤多呈轻中度强化,部分病例动脉期可见局部粘膜线完整;也有部分学者认为呈明显强化,但有缓慢强化的特征。大体标本,GS多表现为黄白色外观,而GIST多表现为暗红色外观或出血表现;免疫组化检测,CD117、CD34、Desmin 和SMA 均为阴性,而S-100呈弥漫强阳性者可确诊,这与GIST相反。 3. 胃平滑肌瘤(gastric leiomyoma,GL):GL是起源于中胚层的良性肿瘤,常无特异性临床症状,病变以单发常见,增大后向粘膜或浆膜面生长,好发于贲门及胃底。GL内镜下表现为半球形隆起或长梭形,因此表现易被误诊为GIST。胃平滑肌肉瘤多从胃固有肌层发生,较为少见。肿瘤的大小并不能作为判断良恶性的指标,有文献报道其强化通常较胃神经鞘瘤明显,尤其在门脉期。良恶性及肿瘤性质的鉴别主要通过术后病理和免疫组化,光镜下胃平滑肌瘤无“淋巴套“样结构,细胞密度大而无分裂象或甚少分裂象;GL标本免疫组化除了SMA和Desmin表现为阳性外,其余免疫学标记物多均为阴性。 4. 胃异位胰腺(gastric ectopic pancereas,GEP)异位胰腺亦称为迷走胰腺或副胰,是正常胰腺以外孤立的胰腺组织,常发生在胃、十二指肠及近段空肠等部位。GEP缺乏临床症状,当并发炎性病变、出血、梗阻时可出现相关临床表现。胃镜下GEP多表现为扁圆形或半球形黏膜下隆起,病灶中央多可见呈特征性脐样凹陷的导管开口,而GS胃镜下多为半球状黏膜隆起,缺乏导管开口。 治疗后0天 胃肠治疗,腹部切口经有最大1.2cmTrocar孔大小,脐周切口取出标本,美容、微创、术后恢复快,疼痛轻。
 葛磊 主任医师 广东医科大学附属医院 胃肠外科121人已读
葛磊 主任医师 广东医科大学附属医院 胃肠外科121人已读 - 医学科普 胃肠镜检查害怕怎么办?葛磊 主任医师 广东医科大学附属医院 胃肠外科1086人已读
- 医学科普 上腹部不适篇之胃溃疡葛磊 主任医师 广东医科大学附属医院 胃肠外科1人已购买
- 医学科普 非肿瘤人群CA72-4单项指标偏高的原因分析葛磊 主任医师 广东医科大学附属医院 胃肠外科11人已购买





